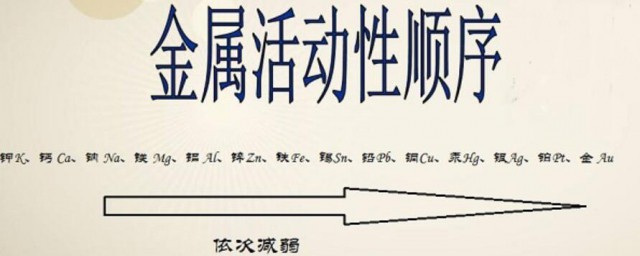
1、金屬活動性順序:
鉀K、鈣Ca、鈉Na、鎂Mg、鋁Al、鋅Zn、鐵Fe、錫Sn、鉛Pb、銅Cu、汞Hg、銀Ag、鉑Pt、金Au,金屬活動性依次減弱。
2、金屬活動性規律:
(1)排在前面的金屬可以將排在後面的金屬從它們的金屬溶液中置換出來。(若金屬過於活潑,則會直接與水反應,並不會與水中的金屬離子反應);
(2)理論上講,金屬活動性表中鐵及排在其前的金屬均可置換出純水中的氫;
(3)若隻考慮氫離子的氧化性,排在氫(H)前的金屬才能和非氧化性酸反應,置換出氫;
(4)排在越後的金屬越容易,也越先從它們的化合物中被置換出來;排在越前的金屬越容易,也越先把其他化合物中的金屬置換出來。