多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病百科
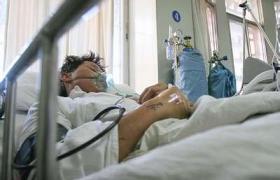
多發性骨髓瘤(multiplemyeloma,MM)是惡性漿細胞病中最常見的一種類型,又稱骨髓瘤、漿細胞骨髓瘤或Kahler病,直到1889年經Kahler詳細報告病例後,多發性骨髓瘤才普遍為人們所瞭解和承認.多發性骨髓瘤的特征是單克隆漿細胞惡性增殖並分泌大量單克隆免疫球蛋白,發病率估計為2~3/10萬,男女比例為1.6:1,大多患者年齡>40歲,黑人患者是白人的2倍.
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病病因
(一)發病原因MM的病因迄今尚未完全明確,臨床觀察,流行病學調查和動物實驗提示,電離輻射,慢性抗原刺激,遺傳因素,病毒感染,基因突變可能與MM的發病有關,MM在遭受原子彈爆炸影響的人群和在職業性接受或治療性接受放射線人群的發病率顯著高於正常,而且接受射線劑量愈高,發病率也愈高,提示電離輻射可誘發本病,其潛伏期較長,有時長達15年以上.
因此遺傳因素、電離輻射、慢性抗原刺激等,均可能與本病的發生有關.
(二)發病機制目前認為MM瘤細胞雖然主要表達B細胞--漿細胞特點,但其起源卻是較前B細胞更早的造血前體細胞(hematopoiesisprecursorcell)的惡變.
至於造血前體細胞發生惡變的機制,目前尚未完全闡明,有眾多證據表明MM的發生與癌基因有關.
淋巴因子細胞因子,生長因子,白細胞介素,集落刺激因子與骨髓瘤的關系在近年來受到重視,B細胞的增生,分化,成熟至漿細胞的過程與多種淋巴因子有關,推測IL-6等淋巴因子分泌的調節異常可能與MM的發病有關,基於此點,有人試用IL-6抗體治療MM,療效尚待評估.
溶骨性病變是MM的重要特征之一,目前認為,溶骨性病變主要並非由瘤細胞直接侵蝕骨質引起,而是由瘤細胞分泌一些因子激活破骨細胞所致,這些因子包括IL-1,淋巴細胞毒素,腫瘤壞死因子(TNF)以及破骨細胞激活因子(OAF),OAF的活性需經IL-1,淋巴細胞毒素,TNF介導,這些因子能夠激活破骨細胞,導致骨質疏松,骨質破壞,另有研究指出,6號染色體長臂缺失可促使TNF,OAF增多,加重溶骨性病變,幹擾素γ和腎上腺皮質激素則可抑制這些因子的產生.
MM的多種多樣的臨床表現是由於惡變克隆漿細胞無節制地增生,浸潤及其分泌的大量單克隆免疫球蛋白所引起:瘤細胞在原發部位骨髓的過度增生,導致骨髓造血功能抑制;瘤細胞廣泛浸潤可累及淋巴結,脾臟,肝臟,呼吸道及其他部位,引起受累組織器官的功能障礙:瘤細胞分泌的一些因子引起溶骨性病變及相關的癥狀;瘤細胞分泌的大量單克隆免疫球蛋白出現於血中引起血液黏度增高及凝血因子功能障礙,而過量輕鏈自腎臟排泄引起腎臟損害,輕鏈沉積於組織器官造成淀粉樣變性損害,而同時正常多克隆漿細胞增生和多克隆免疫球蛋白合成受到抑制,使機體免疫力減低,易招致繼發感染.
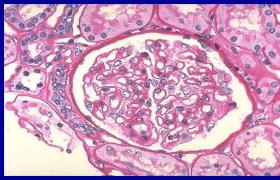
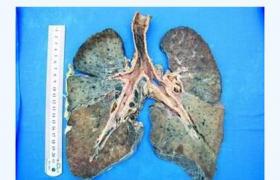
MM最常見侵犯骨骼,病變骨的骨小梁破壞,骨髓腔內為灰白色瘤組織所充塞,骨皮質變薄或被腐蝕破壞,骨質變得軟而脆,可用刀切開,瘤組織切面呈灰白色膠樣,若有出血則呈暗紅色,瘤組織可穿透骨皮質,浸潤骨膜及周圍組織,在顯微鏡下瘤細胞呈彌漫分佈,間質量少,由纖細的纖維組織及薄壁血管組成,小部分腫瘤可有豐富的網狀纖維,瘤細胞是不同分化程度的漿細胞,分化好者酷似正常成熟漿細胞,分化差者類似組織細胞,胞體較大,外形不規則,胞質藍染,核旁空暈不明顯,核大且染色質細致,含1或2個核仁,可見雙核或多核瘤細胞,也有瘤細胞呈灶性分佈者,骨髓外浸潤多見於肝,脾,淋巴結及其他網狀內皮組織,也見於腎,肺,心,甲狀腺,睪丸,卵巢,消化道,子宮,腎上腺及皮下組織,部分病例(8%~15%)的瘤組織及臟器有淀粉樣物質沉著,即免疫球蛋白輕鏈沉著,用剛果紅染色,在普通光學顯微鏡下和旋光顯微鏡下分別呈示特殊綠色和二色性,用免疫熒光法可鑒定其為輕鏈,在此種淀粉樣物質沉著周圍有異物巨細胞反應,常見受累器官為舌,肌肉,消化道,腎,心肌,血管,關節囊及皮膚.
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病症状
多發性骨髓瘤的癥狀:
骨骼腫塊骨痛骨質破壞骨質疏松關節疼痛關節腫脹尿蛋白臨床表現起病緩慢,部分患者可長期無癥狀,但血清蛋白電泳發現有單克隆經過免疫球蛋白(IG)峰,或尿中輕鏈陽性,稱之為“骨髓瘤前期",此期可長達3~5年.主要臨床表現分為以下兩類:
骨髓瘤細胞對各組織浸潤
①對骨骼的浸潤:最常侵犯的骨骼是顱骨,肋骨,胸骨,脊椎和四肢長骨的近側端,由於瘤細胞在骨髓腔內無限增殖,導致彌漫性骨質疏松或限性骨質破壞,骨痛是最常見的早期癥狀,以腰部最為多見,其次為胸骨,肋骨與四肢骨,初起時疼痛可為間發性或遊走性,後漸加重而呈持續性,局部有壓痛,隆起或波動感;可伴發病理性骨折,經常不在負重部位,常有幾處骨折同時發生,X射線檢查可問題發現典型的多發性溶骨性病變,彌漫性骨質疏松,病理性骨折等,有助診斷.
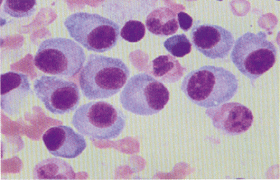
②對骨髓的浸潤:瘤細胞在骨髓內大量增殖,引起骨髓象的明顯改變,增生減低,活躍或明顯活躍,特點是骨髓瘤細胞占10~90%,細胞體積大小不等,直徑15~30μm,卵圓形或圓形,胞漿豐富,呈深藍或亮藍色,可有空泡,核旁透明區不明顯,核圓形或橢圓形,偏於細胞一側,染色質呈粗網狀,含1~2個核仁,大而明顯,有時一細胞內可見2~3個細胞核.成熟紅細胞常呈錢串狀排列,在周圍血象中,表現為進行性正常細胞,正常色素型貧血,在塗片中,紅細胞呈錢串狀,白細胞與血小板計數可正常或偏低,晚期表現為全血細胞減少.
③對其他器官的浸潤:由於脊椎的骨折或骨髓瘤本身對脊神經根的壓迫或對腦和脊髓的浸潤,可引起神經痛,感覺異常,甚至癱瘓,由於瘤細胞在全身的浸潤,使肝,脾,淋巴結腫大,以肝大為多見,亦可侵及其他臟器,引起相應的臨床小組表現,因骨破壞和骨質吸收,大量鈣入血,加之M蛋白與鈣結合使結合鈣增加,可致高鈣血癥和尿鈣增多.
與M蛋白有關的臨床表現有以下各種表現:
①尿蛋白,約40~70%骨髓瘤患者,尿中出現Ig的輕鏈,稱之為本斯·瓊斯氏蛋白,系由於瘤細胞合成的Ig分子中輕鏈多於重鏈,輕鏈分子小,可自腎小球濾過而出現在尿中,輕鏈量少時不易檢出,以濃縮尿作電泳則陽性率高.
②血沉增速,第小時增快至100mm以上.
③出血傾向,血小板減少以及M蛋白引起的血流滯緩,血管壁損害,血小板與凝血因子功能的障礙,患者常有出血傾向,表治療現為粘膜滲血,皮膚紫癜,晚期可有內臟或顱內出血,造成嚴重後果.
④腎功能衰竭,由於輕鏈在腎小管的沉積,高鈣血癥與高尿酸血癥使腎小管重吸收的功能遭受損害,瘤細胞對腎的浸潤等原因,國內慢性腎功能不全是本病顯著的特征之一成為,病程晚期,尿毒癥可成為多種致死的原因.
⑤易受感染,正常Ig含量的減低常導致等獎免疫功能障礙,患者常有反復感染,以肺部和尿路感染較為多見.
⑥高粘滯度綜合征,大量單克隆Ig提高血液粘滯度,使血流遲緩,引起微循環障礙,視網膜,腦,腎等器官尤易受到損傷,引起頭暈,視力障礙,手足麻木等癥狀,嚴重影響大腦功能時可導致昏迷,本綜合征多見於IgM型骨髓瘤和巨球蛋白血癥.
⑦雷諾氏現象,部分患者的單克隆Ig是冷沉淀球蛋白,遇冷時球蛋白凝集沉淀,引起微循環障礙,出現手足紫紺,冰冷,麻木或疼痛等現象,遇熱後癥狀緩解.
⑧淀粉樣變性,少數患者伴發淀粉樣變性,淀粉樣物質廣泛沉積於組織,器官和腫瘤中,引起周圍神經,腎,心,肝,脾的病變導致肝,脾腫大,關節疼痛,神經功能異常等臨床表現.
1.骨痛:骨痛是本病的主要癥狀之一,疼痛程度輕重不一,早期常是輕度的,暫時的,隨著病程進展可以變為持續而嚴重,疼痛劇烈或突然加劇,常提示發生瞭病理性骨折,據北京協和醫院125例MM首發癥狀分析,80例(64.0%)以骨痛為主訴,骨痛部位以腰骶部最常見(28.0%),其次為胸肋骨(27.0%),四肢長骨較少(9.0%),少數患者有肩關節或四肢關節痛,絕大多數(90%~93%)患者在全病程中都會有不同程度的骨痛癥狀,但確有少數患者始終無骨痛.
除骨痛,病理骨折外,還可出現骨骼腫物,瘤細胞自骨髓向外浸潤,侵及骨皮質,骨膜及鄰近組織,形成腫塊,在多發性骨髓瘤,這種骨骼腫塊常為多發性,常見部位是胸肋骨,鎖骨,頭顱骨,鼻骨,下頜骨及其他部位,與孤立性漿細胞瘤不同的是,其病變不僅是多發的,而且骨髓早已受侵犯,並有大量單克隆免疫球蛋白的分泌.
2.貧血及出血傾向:貧血是本病另一常見臨床表現,據北京協和醫院125例分析,絕大多數(90%)患者都在病程中出現程度不一的貧血,其中部分(10.4%)患者是以貧血癥狀為主訴而就診,貧血程度不一,一般病程早期較輕,晚期較重,血紅蛋白可降到<50g/L,造成貧血的主要原因是骨髓中瘤細胞惡性增生,浸潤,排擠瞭造血組織,影響瞭造血功能,此外,腎功不全,反復感染,營養不良等因素也會造成或加重貧血.
出血傾向在本病也不少見,北京協和醫院125例中8例是以出血為首發癥狀而就醫,而在病程中出現出血傾向者可達10%~25%,出血程度一般不嚴重,多表現為黏膜滲血和皮膚紫癜,常見部位為鼻腔,牙齦,皮膚,晚期可能發生內臟出血及顱內出血,導致出血的原因是血小板減少和凝血障礙,血小板減少是因骨髓造血功能受抑,凝血障礙則因大量單克隆免疫球蛋白覆蓋於血小板表面及凝血因子(纖維蛋白原,凝血酶原,因子Ⅴ,Ⅶ,Ⅷ等)表面,影響其功能,造成凝血障礙,免疫球蛋白異常增多使血液黏度增加,血流緩慢不暢,損害毛細血管,也可造成或加重出血.
3.反復感染:本病患者易發生感染,尤以肺炎球菌性肺炎多見,其次是泌尿系感染和敗血癥,病毒感染中以帶狀皰疹,周身性水痘為多見,北京協和醫院125例中以發熱,感染為主訴而就醫者18例(占14.4%),其中多數系肺部感染,部分患者因反復發生肺炎住院,進一步檢查方確診為MM並發肺炎,對晚期MM患者而言,感染是重要致死原因之一,本病易感染的原因是正常多克隆B細胞--漿細胞的增生,分化,成熟受到抑制,正常多克隆免疫球蛋白生成減少,而異常單克隆免疫球蛋白缺乏免疫活性,致使機體免疫力減低,致病菌乘虛而入,此外,T細胞和B細胞數量及功能異常,以及化療藥物和腎上腺皮質激素的應用,也增加瞭發生感染的機會.
4.腎臟損害:腎臟病變是本病比較常見而又具特征性的臨床表現,由於異常單克隆免疫球蛋白過量生成和重鏈與輕鏈的合成失去平衡,過多的輕鏈生成,相對分子質量僅有23000的輕鏈可自腎小球濾過,被腎小管重吸收,過多的輕鏈重吸收造成腎小管損害,此外,高鈣血癥,高尿酸血癥,高黏滯綜合征,淀粉樣變性及腫瘤細胞浸潤,均可造成腎臟損害,患者可有蛋白尿,本-周(Bence-Jones)蛋白尿,鏡下血尿,易被誤診為“腎炎",最終發展為腎功能不全,腎功能衰竭是MM的致死原因之一,在大多數情況下,腎功能衰竭是慢性,漸進性的,但少數情況下可發生急性腎功能衰竭,主要誘因是高鈣血癥和脫水,若處理及時得當,這種急性腎功能衰竭還可逆轉.
5.高鈣血癥:血鈣升高是由於骨質破壞使血鈣逸向血中,腎小管對鈣外分泌減少及單克隆免疫球蛋白與鈣結合的結果,高鈣血癥的發生率報告不一,歐美國傢MM患者在診斷時高鈣血癥的發生率為10%~30%,當病情進展時可達30%~60%,我國MM患者高鈣血癥的發生率約為16%,低於西方國傢,高鈣血癥可引起頭痛,嘔吐,多尿,便秘,重者可致心律失常,昏迷甚至死亡,鈣沉積在腎臟造成腎臟損害,重者可引起急性腎功能衰竭,威脅生命,故需緊急處理.
6.高黏滯綜合征:血中單克隆免疫球蛋白異常增多,一則包裹紅細胞,減低紅細胞表面負電荷之間的排斥力而導致紅細胞發生聚集,二則使血液黏度尤其血清黏度增加,血流不暢,造成微循環障礙,引起一系列臨床表現稱為高黏滯綜合征,常見癥狀有頭暈,頭痛,眼花,視力障礙,肢體麻木,腎功能不全,嚴重影響腦血流循環時可導致意識障礙,癲癇樣發作,甚至昏迷,眼底檢查可見視網膜靜脈擴張呈結袋狀擴張似“香腸",伴有滲血,出血,因免疫球蛋白包裹血小板及凝血因子表面,影響其功能,加之血流滯緩損傷毛細血管壁,故常有出血傾向,尤以黏膜滲血(鼻腔,口腔,胃腸道黏膜)多見,在老年患者,血液黏度增加,貧血,血容量擴增可導致充血性心力衰竭發生,雷諾現象也可發生.
高黏滯綜合征的發生既與血中免疫球蛋白濃度有關,也與免疫球蛋白類型有關,當血液黏度(血漿或血清黏度)超過正常3倍以上,血中單克隆免疫球蛋白濃度超過30g/L時,易發生高黏滯綜合征,在各種免疫球蛋白類型中,IgM相對分子質量大,形狀不對稱,並有聚集傾向,故最易引起高黏滯綜合征,其次,IgA和IgG3易形成多聚體,故也較易引起高黏滯綜合征.
7.高尿酸血癥:血尿酸升高>327μmol/L者在MM常見,北京協和醫院MM91例中,61例(67%)有高尿酸血癥,血尿酸升高是由於瘤細胞分解產生尿酸增多和腎臟排泄尿酸減少的結果,血尿酸升高雖然很少引起明顯臨床癥狀,但可造成腎臟損害,應予預防和處理.
8.神經系統損害:瘤細胞浸潤,瘤塊壓迫,高鈣血癥,高黏滯綜合征,淀粉樣變性以及病理性骨折造成的機械性壓迫,均可成為引起神經系統病變和癥狀的原因,神經系統癥狀多種多樣,既可表現為周圍神經病和神經根綜合征,也可表現為中樞神經系統癥狀,胸椎,腰椎的壓縮性病理性骨折可造成截癱,北京協和醫院125例中12例有神經系統病變,周圍神經病變3例,神經根損害3例,顱內損害2例,脊髓受壓而致截癱4例.
9.淀粉樣變性:免疫球蛋白的輕鏈與多糖的復合物沉淀於組織器官中即是本病的淀粉樣變性,受累的組織器官常較廣泛,舌,腮腺,皮膚,心肌,胃腸道,周圍神經,肝,脾,腎,腎上腺,肺等均可被累及,可引起舌肥大,腮腺腫大,皮膚腫塊或苔蘚病,心肌肥厚,心臟擴大,腹瀉或便秘,外周神經病,肝脾腫大,腎功能不全,等等,淀粉樣變性的診斷依賴組織活檢病理學檢查,包括形態學,剛果紅染色及免疫熒光檢查,歐美國傢報告淀粉樣變性在MM的發生率為10%~15%,而我國的發生率為1.6%~5.6%,由淀粉樣變性損害正中神經引起的“腕管綜合征"(carpaltunnelsyndrome)在西方國傢多見,而國內尚未見有報告.
10.肝脾腫大及其他:瘤細胞浸潤,淀粉樣變性導致肝脾腫大,肝大見於半數以上患者,脾大見於約20%患者,一般為肝,脾輕度腫大,淋巴結一般不腫大,少數患者可有關節疼痛,甚至出現關節腫脹,類風濕樣結節,系骨關節發生淀粉樣變性的表現,皮膚損害如瘙癢,紅斑,壞疽樣膿皮病,多毛僅見於少數患者,個別患者有黃瘤病,據認為是單克隆免疫球蛋白與脂蛋白結合的結果.
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病检查
多發性骨髓瘤檢查項目:
染色體蛋白電泳免疫球蛋白輕鏈酚紅排泄試驗尿素尿酸內生肌酐清除率
實驗室檢查對MM的診斷,分型,臨床分期及預後判斷都有重要意義.
1.外周血:貧血見於絕大多數患者,隨病情進展而加重,一般屬正細胞正色素性貧血,但可有大細胞性貧血伴骨髓幼紅細胞巨幼樣變,也可因有失血而表現小細胞低色素性貧血,紅細胞常呈緡錢狀排列,血沉也明顯加快,常達80~100mm/h以上,此因異常球蛋白包裹紅細胞表面使紅細胞表面負電荷之間排斥力下降而相互聚集的結果,紅細胞聚集現象可能給紅細胞計數,血型檢查造成困難.
白細胞計數正常或減少,白細胞減少與骨髓造血功能受損及白細胞凝集素的存在有關,白細胞分類計數常顯示淋巴細胞相對增多至40%~55%,外周血塗片偶可見到個別瘤細胞,若出現大量瘤細胞,應考慮為漿細胞白血病.
血小板計數正常或減少,血小板減少的原因是骨髓造血功能受抑和血小板凝集素存在的緣故,當血小板表面被異常球蛋白覆蓋時,功能受到影響,可成為出血的原因之一.
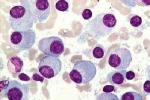
2.骨髓象:骨髓瘤細胞的出現是MM的主要特征,瘤細胞數量多少不等,一般都占有核細胞5%以上,多者可達80%~95%以上,骨髓一般呈增生性骨髓象,各系統比例與瘤細胞數量有關,當瘤細胞所占比例較小時,粒細胞和紅細胞系比例可大致正常,巨核細胞數也可在正常范圍;當瘤細胞數量較多,所占比例較大時,粒細胞系,紅細胞系及巨核細胞均可明顯減少,值得提出的是,在部分患者,特別在病程早期,骨髓瘤細胞可呈灶性分佈,單個部位骨髓穿刺不一定檢出骨髓瘤細胞,此時應作多部位骨髓穿刺或骨髓活檢,方可發現瘤細胞,瘤細胞易位於塗片尾部,應註意檢查塗片尾部.
骨髓瘤細胞形態呈多樣性,分化良好者與正常成熟漿細胞形態相似,分化不良者呈典型骨髓瘤細胞形態,而多數瘤細胞形態似幼漿細胞或漿母細胞形態,同一患者的骨髓中可出現形態不一的骨髓瘤細胞,典型骨髓瘤細胞較成熟漿細胞大,直徑為30~50μm細胞外形不規則,可有偽足,胞質藍染,核旁空暈消失或不明顯,胞質中可見泡壁含核糖核酸,泡內含中性核蛋白的空泡,也可見到含本-周蛋白的類棒狀小體,以及外層含免疫球蛋白,而內含糖蛋白的拉塞爾小體(Ruseu小體),核較大,核染色質細致,有一或兩個核仁,少數瘤細胞具有雙核或多核,但核分裂並不常見,IgA型骨髓瘤細胞胞質經瑞特染色可呈火焰狀,此因嗜堿性糖蛋白被嗜酸性糖蛋白取代的緣故,據觀察,瘤細胞形態近似成熟漿細胞者病程進展較慢,瘤細胞形態呈分化不良者病程進展較快.
在透射電子顯微鏡下,瘤細胞的顯著特征是內質網的增多和擴大,高爾基(Golgi)體極為發達,擴大的粗面內質網內含無定形物,橢圓形小體,這些物質與血清中M蛋白有關,發達的高爾基體內含致密小體和空泡,線粒體也增多,增大,嵴豐富,常可見到胞質內有空泡,拉塞爾小體,結晶體,包涵體,胞核大而圓,常偏於一側,核染色質較粗,核仁大而多形化,有時可見核內包涵體,胞核與胞質發育成熟程度不成比例是瘤細胞在透射電子顯微鏡下的重要特征.
應用抗免疫球蛋白的重鏈抗體和抗免疫球蛋白輕鏈抗體,進行免疫熒光法檢查,可發現骨髓瘤細胞呈陽性,但僅含有一種重鏈和一種輕鏈,與其血清中M蛋白(Mprotein)的重鏈,輕鏈類型一致.
3.血清異常單克隆免疫球蛋白:異常單克隆免疫球蛋白增多引起的高球蛋白血癥是本病的重要特征之一,血清清蛋白減少或正常,A/G比例常倒置,異常單克隆免疫球蛋白大量增多的同時,正常免疫球蛋白常明顯減少,檢測血清異常單克隆免疫球蛋白的方法有下述幾種:
(1)血清蛋白醋酸纖維薄膜電泳:異常增多的單克隆免疫球蛋白表現為一濃集的窄帶,經密度掃描儀繪出的圖像表現為一窄底高峰,其峰高度至少較峰底寬度大2倍以上,即M成分(或稱M蛋白),這是由於單克隆免疫球蛋白的相對分子質量大小,氨基酸組成,所帶電荷完全相同,因而在電場的泳動速度完全相同的緣故,M成分可出現在γ區(IgG,IgM),β或α2區(IgA),這取決於單克隆免疫球蛋白的類型,當M成分顯著增多時,其他免疫球蛋白及血清清蛋白常明顯減少.
(2)免疫電泳:單克隆免疫球蛋白在免疫電泳上表現為異常沉淀弧,在出現一種異常重鏈沉淀弧和一種異常輕鏈沉淀弧的同時,另一種輕鏈和其他類型重鏈常明顯減少,根據免疫電泳結果可以確定單克隆免疫球蛋白類型,從而對多發性骨髓瘤進行分型,即IgG型,IgA型,IgM型,IgD型,IgE型,輕鏈型,雙克隆或多克隆型,不分泌型.
(3)聚合酶鏈反應(PCR):近年來采用PCR技術檢測免疫球蛋白重鏈基因重排作為單克隆B細胞--漿細胞惡性增生的標記,用於本病的診斷及與良性反應性免疫球蛋白增多的鑒別診斷,用上述方法檢出單克隆免疫球蛋白後,尚需進行定量,目前多采用速率散射比濁法(ratenephelometry)確定免疫球蛋白濃度.
4.尿液:常規檢查常發現有蛋白尿,鏡下血尿,但管型少見,有時可見到漿(瘤)細胞,具有診斷意義的是尿中出現本周蛋白,又稱凝溶蛋白,該蛋白在酸化的尿液中加熱至50~60℃時發生凝固,但進一步加熱則又溶解,本-周蛋白就是自腎臟排出的免疫球蛋白輕鏈,在多發性骨髓瘤,瘤細胞不僅合成和分泌大量單克隆免疫球蛋白,而且重鏈與輕鏈的合成比例失調,往往有過多輕鏈生成,故血中輕鏈濃度明顯升高,輕鏈的相對分子質量僅23000,可通過腎小球基底膜而排出,故出現本-周蛋白尿,由於單克隆漿(瘤)細胞儀能合成一種輕鏈(κ或λ鏈),故本-周蛋白僅為一種輕鏈,應用免疫電泳可確定本-周蛋白為何種輕鏈,近年來采用速率散射比濁法定量測定尿中輕鏈含量,顯著提高瞭尿液輕鏈檢測的敏感度和精確度,既往用酸加熱法檢測本-周蛋白的陽性率為30%~60%,且有假陽性,而采用尿液輕鏈定量法的陽性率幾近100%,且不出現假陽性,正常人尿中有κ和λ兩種輕鏈,含量均低,尿中出現大量單一輕鏈,而另一種輕鏈含量減低甚至檢測不出,是MM的特征之一.
5.腎功能:腎功能常受損,尤多見於病程中期,晚期,血肌酐,尿素氮,內生肌酐清除率測定,酚紅排泄試驗,放射性核素腎圖等檢查可確定腎功能是否受損及受損程度,晚期可發生尿毒癥,成為死因之一,當患者有大量本-周蛋白尿時,應避免進行靜脈腎盂造影,因造影劑可能與本-周蛋白發生反應而導致急性腎功能衰竭.
6.血液生化異常:血鈣常升高,國外報告高鈣血癥在MM的發生率為30%~60%,國內報告發生率為15%~20%,血磷一般正常,腎功能不全時磷排出減少可引起血磷升高,膽固醇可正常,升高或降低,高膽固醇血癥多見於IgA型骨髓瘤,低膽固醇血癥多見於IgG型骨髓瘤,堿性磷酸酶可正常,降低或升高,既往曾認為本病有骨質破壞而無成骨過程,故堿性磷酸酶不升高,並以此作為本病與甲狀旁腺功能亢進,骨轉移癌的鑒別點之一,但近年來國內外均有研究證明並非所有MM患者均無成骨活動,部分患者的堿性磷酸酶水平可高於正常,故不可憑借堿性磷酸酶水平升高排除本病,高尿酸血癥在本病常見,可並發泌尿道結石.
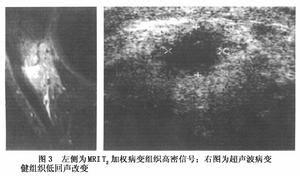
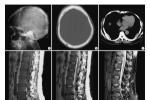
7.X射線及其他影像學檢查:X射線檢查在本病診斷上具有重要意義,本病的X射線表現有下述4種:①彌漫性骨質疏松:瘤細胞浸潤及瘤細胞分泌激活破骨細胞的因子(IL-1,淋巴細胞毒素,TNF,OAF)引起普遍性骨質疏松,脊椎骨,肋骨,盆骨,顱骨常表現明顯,也可見於四肢長骨,②溶骨性病變:骨質疏松病變的進一步發展即造成溶骨性病變,多發性圓形或卵圓形,邊緣清晰銳利似穿鑿樣溶骨性病變是本病的典型X射線征象,常見於顱骨,盆骨,肋骨,脊椎骨,偶見於四肢骨骼,③病理性骨折:骨折在骨質破壞的基礎上發生,最常見於下胸椎和上腰椎,多表現為壓縮性骨折,其次見於肋骨,鎖骨,盆骨,偶見於四肢骨骼,④骨質硬化:此種病變少見,一般表現為局限性骨質硬化,出現在溶骨性病變周圍,彌漫性骨質硬化罕見,IgD型骨髓瘤較易並發骨質硬化,γ-骨顯像是近年來用於檢查骨質異常的手段之一,在本病,溶骨性病變表現為病變部位有放射線濃集,此法可一次顯示周身骨骼,且較X射線敏感,X射線僅在骨骼脫鈣達30%以上時才能顯示出病變,而γ-骨顯像在病變早期即可出現放射線濃集征象,但值得指出的是,γ-骨顯像雖然敏感性較高,但特異性卻不高,任何原因引起的骨質代謝增高均可導致放射線濃集征象,故應註意鑒別,CT和磁共振成像(MRI)也用於本病的診斷性檢查,特別當骨髓瘤侵犯中樞神經系統或脊椎骨壓縮性骨折損傷脊髓,神經根時,CT及(或)MRI檢查可為診斷提供重要信息.
8.B超:腎功能損害,泌尿結石,心肌肥厚者可提示.
9.放射性核素:腎圖檢查可確定腎功能損害程度.
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病预防
本病的發生與環境,飲食等因素有關,故預防本病發生,增強病人的體質,積極治療慢性疾患,避免射線及化學毒物的接觸,對於疾病的防治具有重要的意義.
首先應避免與致癌因素接觸,若有接觸史或病狀可疑者,應定期體檢,爭取早期發現及時治療,患者宜參加適當的經常性活動,以減少脫鈣,註意個人衛生,防止感染,尤其要註意口腔粘膜和皮膚的清潔,防止感冒.
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病治疗
(一)治療
1.支持治療:支持治療在本病的治療上占有重要地位,不容忽視.
長期臥床患者容易發生骨骼脫鈣,高鈣血癥,腎功不全,鼓勵患者進行適當的經常性活動有助於改善上述狀況,若骨痛限制活動時,可予止痛劑或局部放射達到止痛效果,胸肋骨或胸腰椎有病變者,應配用輕便矯正性支架加以保護,既可減輕疼痛,又可防止病理性骨折,對已有嚴重胸和(或)腰椎壓縮性骨折並有可能損及脊髓而截癱患者,需限制活動,胸椎,腰椎有溶骨性病變患者應睡鋪有軟墊的木板硬床,防止脊柱彎曲過度引起骨折而損傷脊髓.
貧血應得到改善或糾正,輸紅細胞使血紅蛋白濃度維持在80g/L以上,以改善患者一般情況,使之能夠耐受化療,紅細胞生成素(erythropoietin,EPO)皮下或靜脈註射有助於改善貧血,血小板減少引起出血時,可輸濃縮血小板懸液,當高黏滯綜合征嚴重時,可采用血漿交換法,迅速去除異常大量免疫球蛋白,降低血漿黏滯度,緩解癥狀,高鈣血癥用靜脈註射降鈣素(calcitonin)5~10U/(kg·d),靜脈滴註帕米膦酸二鈉(博寧,阿可達)60~90mg/d,口服潑尼松(60mg/d)可有效降低血鈣,高尿酸血癥者口服別嘌醇(allopurinol)300~600mg/d可有效降低血尿酸水平,脫水是由尿鈣增多引起多尿,腎小管功能不全引起多尿以及高鈣血癥引起嘔吐等因素所造成,治療上一方面給予補液,使尿量達到1500~2000ml/d,另一方面及時處理高鈣血癥,對腎功能不全患者,按腎功能不全治療原則處理.
①血紅蛋白低於60g/L,輸註紅細胞;②高鈣血癥:等滲鹽水水化,強的松:20mg,口服,3~4次/d;③高尿酸血癥:別嘌呤醇:0.2mg,口服,3次/d;④高粘滯血癥:血漿交換治療;⑤腎功能衰竭:血液透析;⑥感染:聯合應用抗生素治療,對反復感染的病人用青黴素,丙種球蛋白預防性註射有效.
本病患者易並發感染,應註意預防感冒,保持口腔衛生,一旦發生感染,應針對病原菌選用有效抗生素,力求早期控制感染,肌內註射人血丙種球蛋白難以達到有效預防感染作用,靜脈輸註大劑量人血丙種球蛋白在本病預防和治療感染的作用尚在研究之中.
2.化療:化療是本病的主要治療手段,新化療藥物的應用和用藥方法的改進是近年來本病療效提高的關鍵因素.
作為單藥治療,苯丙氨酸氮芥(米爾法蘭,左旋苯丙氨酸氮芥),環磷酰胺,氮甲(甲酰溶肉瘤素,N-甲),丙卡巴肼(甲基芐肼),卡莫司汀(雙氯乙亞硝脲,卡氮芥,BCNU),洛莫司汀(氯乙環己基亞硝脲,羅氮芥,CCNU),長春新堿,多柔比星(阿黴素),依托泊苷(足葉乙甙,VPl6)等均有療效.
(1)方案:應用最久,療效較好的是應用聯合化療.
①MP方案:苯丙氨酸氮芥(馬爾法蘭)8mg/m2,口服,第l~4天(或4mg/m2,口服,第1~7天);潑尼松60~80mg,口服,第1~7天,4周為1療程,MP的有效率約為50%,中數生存期24~30個月,80%患者在5年內死亡.
②M2方案:卡莫司汀(卡氮芥)00.5mg/kg,靜註,第1天;環磷酰胺10mg/kg,靜註,第1天;苯丙氨酸氮芥(馬爾法蘭)0.25mg/kg,口服,第l~4天;潑尼松1mg/kg,口服,第1~7天,0.5mg/kg,口服,第8~14天;長春新堿0.03mg/kg,靜註,第21天,5周為1療程.
③VBMCP方案:長春新堿1.2mg/m2,靜註,第1天;卡莫司汀(卡氮芥)20mg/m2,靜註,第1天;苯丙氨酸氮芥(馬爾法蘭)8mg/m2,口服,第l~4天;環磷酰胺400mg/m2,靜註,第1天;潑尼松40mg/m2,口服,第1~7天,20mg/m2,口服,第8~14天,5周為一療程.
④VMCP/VBAP方案:長春新堿1mg/m2,靜註,第1天,苯丙氨酸氮芥(馬爾法蘭)6mg/m2,口服,第l~4天,環磷酰胺125mg/m2,口服,第l~4天,潑尼松60mg/m2,口服,第l~4天,3周為一療程;長春新堿1mg/m2,靜註,第1天;卡莫司汀(卡氮芥)30mg/m2,靜註,第1天;多柔比星(阿黴素)30mg/m2,靜註,第1天;潑尼松60mg/m2,口服,第l~4天,3周為1療程,兩個方案交替使用.
(2)目前對難治性病例多采用VAD方案或大劑量苯丙氨酸氮芥(馬爾法蘭)(HDM)方案治療.
①VAD方案:長春新堿0.4mg/24h持續靜脈滴入4天,多柔比星(阿黴素)10mg/(m2·24h)持續靜脈滴入4天,地塞米松40mg,口服,第1~4天,第9~12天,第17~20天,25天為1療程,此方案對難治性病例的有效率為45%~66%,中數生存期11~16個月,主要副作用是大劑量地塞米松招致的繼發性感染,對證實有多藥耐藥基因高表達的難治性病例,可在化療的同時加用MDR逆轉劑,即維拉帕米(異博定)40~80mg口服,3次/d,或環孢素4mg/kg,靜註,2次/d,第1~3天,2.5mg/kg靜註,2次/d,第4~5天,也可1∶3服,環孢素(CsA)5mg/(kg·d).
②大劑量苯丙氨酸氮芥(馬爾法蘭)方案:苯丙氨酸氮芥(馬爾法蘭)50~100mg/m2,靜註,第1天,此方案的有效率約40%,主要副作用是骨髓抑制,需加以註意.
除上述VAD,VAD加MDR逆轉劑和HDM方案外,對難治性病例尚可選擇CBV(環磷酰胺,卡莫司汀(卡氮芥),依托泊苷(足葉乙甙))方案或EDAP(依托泊苷(足葉乙甙),地塞米松,多柔比星(阿黴素),順鉑)方案,兩者的有效率均約40%,有報道大環內酯類抗生素克拉黴素(clarithromycin)500mg,2次/d對本病有效,甚至對化療耐藥的病例也可能奏效,口服沙利度胺(反應停)由200mg/d逐漸增至400~800mg/d,用藥6周以上,有效率約為30%,副作用有嗜睡,便秘,乏力,周圍神經病等.
關於維持治療,在20世紀70年代末期和80年代曾采用MP或聯合用藥方案間歇治療作為化療取得完全緩解後的長期維持治療,但均未能取得明顯延長緩解期的肯定效果,這是由於殘留瘤細胞多系耐藥細胞,故化療難以奏效,近年來研究免疫治療,例如將患者瘤細胞與其樹突狀細胞(Dendriticcell)在體外融合,制成瘤苗,接種於緩解期患者,期望激活患者免疫效應細胞,殺傷殘留的MM細胞.
3.幹擾素及其他生物反應調節劑:幹擾素是具有抗病毒,影響(抑制或刺激)細胞生長,調節免疫等多種功能的細胞因子,幹擾素對細胞(包括腫瘤細胞)生長的影響多表現為抑制作用,同時幹擾素也有激活自然殺傷細胞,激活細胞毒性T細胞,刺激B細胞合成免疫球蛋白等調節免疫作用,因此被用於腫瘤包括本病的治療,應用幹擾素α(3~5)×106U皮下註射,1周3次,至少6周以上,單藥治療本病初治患者的有效率為10%~20%,多為部分緩解,若與化療合並使用,是否優於單用化療尚有爭論,雖然較多報告肯定化療合並幹擾素α可提高緩解率和延長緩解期,但部分報告認為加用幹擾素α對療效並無影響,至於難治性病例,各傢報告均認為幹擾素α很難奏效,對於化療取得完全緩解後患者的維持治療,雖然部分研究報告持否定態度,但是多數研究肯定應用幹擾素α[(3~5)×106U皮下註射,1周3次,長期註射]作為維持治療,可以獲得延長緩解期的效果,此一爭論尚待進一步研究澄清.
白介素6(IL-6)是誘導B細胞分化和刺激B細胞-漿細胞生長的重要細胞因子,人骨髓瘤細胞體外培養需要IL-6,骨髓瘤患者骨髓中及血清中IL-6水平也顯著升高,這些都提示IL-6在本病的發病機制中起著重要作用,因此有研究應用抗IL-6單克隆抗體治療本病,初步報告有一定療效,但有待進一步研究證實.
骨痛是本病的主要癥狀之一,帕米膦酸二鈉(博寧,阿可達)通過抑制破骨細胞活性而減輕骨痛和溶骨性病變,用法為60~90mg,靜脈滴註,每月1次,可重復使用,新近報道應用OAF抑制劑(SD-7784,Statins)治療溶骨性病變,已進入臨床試驗.
有研究報告維A酸通過對IL-6受體的負調控,抑制骨髓瘤細胞生長,而取得一定療效,對血清IL-6水平升高患者口服維A酸治療的研究仍在進行之中.
4.放射治療:放射治療適用於不宜手術切除的孤立性骨漿細胞瘤和髓外漿細胞瘤的治療,同時也是減輕局部劇烈骨痛的有效治療手段,此外,對於化療無效的復發性或耐藥性患者采用半身放療或半身放療加聯合化療,有效率約為50%,放射劑量一般為上半身625cGy,或下半身850cGy,近年來由於骨髓移植的進展,周身放療多作為移植前預處理措施之一,而不再單獨使用.
5.手術治療:當胸椎或腰椎發生溶骨性病變使患者臥床不起並可能因發生壓縮性骨折而導致截癱時,可以進行病椎切除,人工椎體置換固定術,成功的手術將使患者避免發生截癱,在一定程度上恢復活動能力,提高生命質量.
6.造血幹細胞移植:化療雖在本病取得瞭顯著療效,但未能治愈本病,故自20世紀80年代起試用骨髓移植配合超劑量化療和周身放射根治本病,同基因,異基因,自身骨髓(包括外周血幹細胞)移植均已應用於本病的臨床治療.
骨髓移植前的預處理目的在於清除患者體內的瘤細胞並抑制患者的免疫能力使骨髓容易植活,對於本病,多采用大劑量苯丙氨酸氮芥(馬爾法蘭)140~200mg/m2(-2天)和周身放射(TBI)850cGy(-1天)作為預處理,也有采用卡莫司汀(卡氮芥)120mg/m2(-8天),依托泊苷(足葉乙甙)250mg/m2(-8天,-6天),苯丙氨酸氮芥(馬爾法蘭)140mg/m2(-2天)和TBI850cGy(-1天)作為預處理,近年來的總結性研究認為,單用苯丙氨酸氮芥(馬爾法蘭)200mg/m2作為預處理效果相對較好,①同基因骨髓移植:美國西雅圖研究中心報告7例本病患者接受瞭同卵雙生兄弟的同基因骨髓移植,其中2例已分別無病生存8年和15年以上(1994),瑞典報告6例同基因骨髓移植,其中3例已存活6年以上,表明骨髓移植可能治愈本病,②異基因骨髓移植:歐洲骨髓移植組織報告90例,美國西雅圖組報告50例,意大利報告27例,加拿大報告17例本病患者接受瞭異基因骨髓移植,結果相近:4年生存率約30%,10年生存率約20%,但移植相關病死率高達40%~50%,對異基因骨髓移植後復發患者輸註供者去CD8的T淋巴細胞,產生移植物抗腫瘤效應(GVL)可能使部分患者重獲緩解,目前一般認為,異基因骨髓移植對本病雖有肯定療效並有望治愈部分患者,但此療法有一定的危險性,特別是移植物抗宿主病(GVHD)的發生率和骨髓移植相關病死率較高,故應註意選擇合適病例進行異基因骨髓移植,多數學者主張對年齡55歲以下,有HLA相合血緣相關供髓者,預後較差的本病患者應爭取盡早進行骨髓移植,而對具有上述條件但預後較好的患者,則應推遲至第1次復發時再進行骨髓移植,③自體骨髓移植:由於目前采用的預處理方案難於保證徹底清除患者體內瘤細胞,同時又缺少有效的體外凈化骨髓的方法,因而進行自體骨髓移植後的復發率較高,療效有限,雖有研究報告肯定自體骨髓移植可提高緩解率,但對能否延長緩解期則無定論,自體骨髓移植對本病療效的提高有賴於預處理方案的改進和體外骨髓凈化研究的進展,④自體外周血幹細胞移植:本病患者外周血中僅有少量瘤細胞是應用此法治療本病的有利之處,通常在化療後骨髓造血功能恢復早期,配合應用G-CSF等細胞因子動員骨髓造血幹細胞逸入外周血收集並儲存外周血幹細胞,待患者接受大劑量化療和TBI後,再回輸給患者,不同醫療中心報告的療效有所不同,一般認為,無論在緩解率抑或在無病生存期方面自體外周血幹細胞移植可能優於單純化療,但最終難免復發,對此療法的研究,目前正在積極進行之中.
7.CD20單克隆抗體治療:多發性骨髓瘤利妥昔單抗(美羅華)375mg/m2,1次/周×4周,共用4次為1個周期,間歇6個月進行第2個周期,總共6個周期,給利妥昔單抗(美羅華)的第35天予苯丙氨酸氮芥(馬爾法蘭)0.25mg/kg,口服,第1~4天,潑尼松100mg,口服,第1~4天,每4~6周重復1次.
療效判斷標準:判斷本病療效的重要指標是:血清M蛋白和(或)尿本-周蛋白減少50%以上,漿細胞瘤兩個最大直徑縮小50%以上及骨骼溶骨性損害改善,次要標準,骨髓中漿(瘤)細胞減少<5%,血紅蛋白增加20g/L,血鈣及尿素氮降至正常水平,凡經治療後,M蛋白消失,其他上述各項指標均可達到正常水平者為完全緩解達到至少1項,主要指標和至少2項次要指標者為部分緩解,完全緩解率和部分緩解率之和為總有效率.
(二)預後
與本病預後有關的因素有:臨床分期(包括腎功能),免疫球蛋白分型,漿(瘤)細胞分化程度,血清β2-微球蛋白水平,血清乳酸脫氫酶水平以及漿細胞標記指數,臨床分期IA的中數生存期可達5年,而臨床分期ⅢB的中數生存期則短於2年,免疫球蛋白類型對預後也有影響,輕鏈型預後較差,IgA型預後也遜於IgG型,漿(瘤)細胞分化不良者預後劣於漿(瘤)細胞分化較好者,β2-微球蛋白(β2-microglobulin,β2-M)系低相對分子質量(11800)蛋白,是HLA-A,B,C組織相容性抗原復合物的輕鏈部分,正常血清β2-M含量<2.7mg/L,幾乎全部由腎臟排出,近端腎小管以胞飲形式攝取,在腎小管細胞溶酶體降解為氨基酸,在本病由於瘤細胞增生,細胞周轉加速及腎功能損害而導致血,尿β2-M水平升高,目前公認β2-M是本病的重要預後因素,血清β2-M明顯升高為高危因素之一,血清乳酸脫氫酶(LDH)水平升高由組織壞死釋放引起,見於多種炎癥,組織或腫瘤壞死,雖不具特異性,但LDH明顯升高是本病的另一高危因素,漿細胞標記指數(plasmacelllabellingindex,PCL1)代表漿(瘤)細胞合成DNA狀況,反映骨髓瘤進展狀態,PCLI<1.0屬低危組,PCLI<3.0表示骨髓瘤處進展狀態,屬高危組,此外,對於C反應蛋白(CRP)和胸苷激酶(thymidinekinase,TK)是否為獨立的具有預後意義的因素,目前存在不同意見,尚無定論.
本病的病程在不同患者之間有很大差異,按上述預後因素分析,可將本病患者分為低危組,中危組和高危組,目前尚無公認的,統一的劃分標準,下述劃分標準僅作為參考,低危組在診斷時臨床分期為Ⅰ期,如β2-M<2.7mg/L,PCLI<1%,此組中數生存期>5年;中危組在診斷時臨床分期為Ⅱ期,β2-M≥2.7mg/L或PCLI≥1%,此組中數生存期約為3年;高危組在診斷時臨床分期為Ⅲ期,β2-M≥2.7mg/L,同時PCLI≥1%,此組中數生存期約為1年半,就本病總體而言,在目前的以化療為主要治療的條件下,本病患者的中數生存期為30~36個月,導致患者死亡的主要原因是感染,腎功能衰竭,骨髓瘤進展所致周身衰竭或多器官衰竭,少數患者因胃腸道或顱內出血而死亡,約有5%患者轉變為急性白血病,多為急性漿細胞白血病,但也可為急性單核細胞白血病,急性粒-單核細胞白細胞或急性粒細胞白血病.
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病饮食
飲食宜清淡,選用抑制骨髓過度增生的食品,如海帶、紫菜、裙帶萊、海蛤、杏仁.對癥選用抗血栓、補血、壯骨和減輕脾腫大的食品,穩定期可長期服用"康血寧"藥茶.
①抑制骨髓過度增生食療方桃花魚片:青魚肉適量,桃仁酥10g.魚肉切絲,共炒熟即可.適用於各型多發性骨髓瘤.
②抗血栓食療方山楂甜羹:山楂50g,紅花50g.煮羹作點心食.適用於伴有高粘滯血癥的多發性骨髓瘤患者.
③補血、抗消耗食療方
黃芪銀耳湯:黃芪9g,銀耳12g,加水300ml,文火煮1小時加冰糖適量,每日服一次.治療多發性骨髓瘤緩解期,氣陰虛,口幹,盜汗,失眠者.
以上資料僅供參考,詳情請詢醫生.
多發性骨髓瘤 骨髓瘤 赫珀特病 漿細胞骨髓 赫珀特氏病并发症
多發性骨髓瘤並發癥
1.骨折:病理性骨折,常見於顱骨,盆骨,肋骨,脊柱骨骨折等.
2.高鈣血癥:骨髓瘤合並高鈣血癥在歐美患者中的發生率可達30%~60%,臨床可表現為食欲不振,惡心,嘔吐,煩渴性多尿,昏迷.
3.腎臟損害:是MM常見和重要的並發癥,也是患者死亡的主要原因之一,急,慢性腎功能衰竭是多發性骨髓瘤的重要並發癥之一,也是診斷上的重要線索,它可發生在多發性骨髓瘤的任何階段.
4.高黏滯綜合征:在MM患者中發生率為10%,常表現視力下降,意識障礙,中樞神經系統紊亂,心衰等.
5.血液系統並發癥:貧血,出血,血栓.
6.感染:在病程中可反復出現感染,發熱,如皮膚感染,肺部感染等.
7.淀粉樣變性:引起相應的臨床表現,包括舌肥大,腮腺腫大,心肌肥厚,心臟擴大,腹瀉,外周神經病,肝脾腫大等.
8.神經系統損害:MM合並神經系統損害的發病率28.6%~40%,包括脊髓壓迫,神經根脊髓壓迫等.
2/2 首页 上一页 1 2