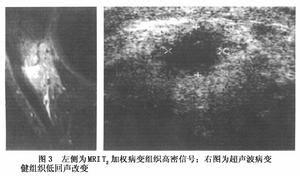
糖原累積病 GDS 糖原累積病
糖原累積病 GDS 糖原累積病百科
糖原累積病是一類由於先天性酶缺陷所造成的糖原代謝障礙疾病.根據歐洲資料,其發病率為1/(2萬~2.5萬).糖原合成和分解代謝中所必需的各種酶至少有8種,由於這些酶缺陷所造成的臨床疾病有12型,其中Ⅰ、Ⅲ、Ⅳ、Ⅵ、Ⅸ型以肝臟病變為主;Ⅱ、Ⅴ、Ⅶ型以肌肉組織受損為主.這類疾病有一個共同的生化特征,即是糖原貯存異常,絕大多數是糖原在肝臟、肌肉、腎臟等組織中貯積量增加.僅少數病種的糖原貯積量正常,而糖原的分子結構異常.
糖原累積病 GDS 糖原累積病
糖原累積病 GDS 糖原累積病病因
遺傳因素(90%)
常染色體隱性遺傳,磷酸化酶激酶缺乏型則是X-性連鎖遺傳.糖原積累病是由於患者缺乏糖原合成和分解過程中所需的酶,使糖原合成或分解發生障礙,導致糖原沉積於組織中而致病,由於酶缺陷的種類不同,造成多種類型的糖原代謝病.
發病機制
糖原是由葡萄糖單位構成的高分子多糖,主要貯存在肝和肌肉中作為備用能量,正常肝和肌肉分別含有約4%和2%糖原,攝人體內的葡萄糖在葡萄糖激酶,葡糖磷酸變位酶和尿苷二磷酸葡糖焦磷酸化酶的催化下形成尿苷二磷酸葡萄糖(UDPG),然後由糖原合成酶將UDPG提供的葡萄糖分子以α-1,4-糖苷鍵連接成一個長鏈,每隔3~5個葡萄糖殘基由分支酶將1,4位連接的葡萄糖轉移成1,6位連接,形成分支,如是擴展,最終構成樹狀結構的大分子,糖原的分子量高達數百萬以上,其最外層的葡萄糖直鏈較長,大多為10~15個葡萄糖單位,糖原的分解主要由磷酸化酶催化,從糖原分子中釋放1-磷酸葡萄糖,但磷酸化酶的作用僅限於1,4糖苷鍵,並且當分枝點前僅存4個葡萄糖殘基時就必須由脫枝酶(淀粉1,6-葡糖苷酶,amyol-1,6-glucosidase)將其中的三個殘基轉移至其他直鏈以保證磷酸化酶的作用繼續進行,與此同時,脫枝酶可以解除α-l,6-糖苷鍵連接的一個葡萄糖分子,這樣反復進行便保證瞭機體對葡萄糖的需求,存在於溶酶體中的α-1,4葡糖苷酶(酸性麥芽糖酶)也能水解不同長度的葡萄糖直鏈,使之成為麥芽糖等低聚糖分子,GSD是由於患者缺乏上述糖原合成和分解過程中任一酶的缺陷使糖原合成或分解發生障礙,導致糖原沉積於組織中而致病,由於酶缺陷的種類不同,造成多種類型的糖原代謝病,常見類型見表,其中Ⅰ,Ⅲ,Ⅵ,Ⅸ型以肝臟病變為主,Ⅱ,Ⅴ,Ⅶ型以肌肉組織受損為主.
糖原累積病 GDS 糖原累積病
糖原累積病 GDS 糖原累積病症状
糖原累積病的癥狀
低血糖癥肝大而硬肝臟腫大生長緩慢酮癥酸中毒無力
本病系遺傳性疾病,患兒出生時就有肝臟腫大,隨著年齡的增長,出現明顯低血糖癥狀,如軟弱無力,出汗,嘔吐,驚厥和昏迷,並可以出現酮癥酸中毒,患兒生長發育遲緩,智力無障礙,體型矮小,肥胖,皮膚顏色淡黃,腹部膨隆,肝臟顯著增大,質地堅硬,肌肉發育差,無力,尤其以下肢最為顯著,多數患此病癥者不能存活至成年,往往死於酸中毒昏迷,輕癥病例在成年後可以獲得好轉,目前本病可區分為十多個亞型,其中以Ⅰ型最為常見.
糖原累積病 GDS 糖原累積病
糖原累積病 GDS 糖原累積病检查
糖原累積病檢查項目
染色體血氨尿酸血清膽固醇果糖耐量試驗血常規肝臟超聲檢查
1、生化檢查:Ⅰ型患者空腹血糖降低至2.24~2.36mmol/L,乳酸及血糖原含量增高,血脂酸,尿酸值升高.
2、白細胞酶的測定:對Ⅲ,Ⅳ,Ⅵ,Ⅸ型病人可能有幫助.
3、糖代謝功能試驗
腎上腺素耐量試驗註射腎上腺素60分鐘後,0,Ⅰ,Ⅲ,Ⅻ型患者血糖均不升高.
胰高血糖素試驗0,Ⅰ,Ⅲ,Ⅳ型患者示血糖反應低平,餐後1~2小時重復此試驗,O,Ⅲ型血糖可轉為正常.
果糖或半乳糖變為葡萄糖試驗Ⅰ型患者在負荷果糖或半乳糖時不能使葡萄糖升高,但乳酸明顯上升.
糖耐量試驗呈現典型糖尿病特征.
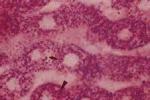
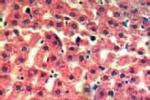
4、肌肉組織或肝組織活檢:活檢組織作糖原定量和酶活性測定,可作為確診的依據,但損傷性大.
5、分子生物學檢測:目前研究較多的為葡萄糖-6-磷酸酶(G-6-Pase)基因,G-6-Pase缺乏可引起Ⅰ型GSD,G-6-Pase基因位於第17號染色體,全長12.5Kb,包含5個外顯子,目前已檢測出多種G-6-Pase基因突變,其中最多見於R83C和Q347X,約占Ⅰ型GSD的60%,但有地區差異,中國人群以nt327G→A(R83H)檢出頻率最高,其次為nt326G→A(R83C),因此G-6-Pase基因第83密碼子上的CpG似乎是突變的熱點,應用PCR結合DNA序列分析或ASO雜交方法能正確地鑒定.88%Ⅰ型糖原累積癥患者攜帶的突變等位基因,基因檢測可避免侵害性的組織活檢,亦可用於攜帶者的檢出和產前診斷.
糖原累積病 GDS 糖原累積病预防
本病屬於遺傳性疾病,尚不能根治,治療主要是延緩病情的發展,增加肌力,改善呼吸困難等癥狀,改善生存質量,現在所能做的預防措施是嚴格遵行“非近親結婚”的婚姻法條例,減少此種病患兒的出生率,提高人們的身體素質,提供人們的生活質量.
遺傳咨詢
對於有傢族病史的要遺傳咨詢可以幫助患病成人進行選擇性生育.
婚前檢查:包括詳細詢問男女雙方及其傢庭成員的健康狀況既往病史及醫治情況,尤其是有無先天畸形,遺傳病史和近親婚配史.應進行傢系調查、血型檢查染色體檢查或基因診斷,以檢出攜帶者.
產前咨詢:孕婦:孕期用藥要經醫生的指導.做好產前的檢查.患者生子女必須進行產前診斷.在妊娠期穿刺羊水進行檢查:
①在羊水中可發現黏多糖增多(但在妊娠16周以前並無診斷意義).
②羊水細胞培養後,對成維細胞進行分析,可做出早期診斷,從而早期終止妊娠.
糖原累積病 GDS 糖原累積病治疗
治療(僅供參考,詳細請詢問醫生)
一、飲食治療:主要用於有肝臟受累、易發生低血糖、酮中毒和乳酸中毒的新生兒和兒童患者.
二、酶替代治療:酶替代治療目前正處於動物實驗階段.酶替代治療是否可用於人,還需作進一步作臨床試驗.特異性酶替代治療可有兩種不同的形式.一種是直接給體內輸入經過微包裹的酶,此為直接法.另一種則為間接法,即利用反轉錄病毒進行轉基因處理,使患者自體的周圍血淋巴細胞或骨髓造血祖細胞逆向轉化為含有正常酶基因的細胞,或通過骨髓移植給患者體內植入含有正常酶基因的骨髓細胞,從而使患者體內可以自身合成所缺乏的黏多糖代謝酶.目前,已有針對I、II、VI型患者的酶替代療法,並在歐美一些國傢正式上市,例如治療粘多糖貯積癥I型的α-L-艾杜糖醛酸酶和治療粘多糖貯積癥II型的艾杜糖硫酸酯酶,但在我國尚未註冊.
三、基因治療:基因治療是治療糖原累積病最有效最徹底的方法,隨著基因工程研究備受關註而迅速發展,糖原累積病所缺乏的酶可用基因工程合成,並選用適當的載體傳輸到特定部位是酶活性恢復,但目前尚未應用於臨床.
四、手術治療:手術治療包括肝腺瘤切除術、部分肝切除術以及器官移植(肝移植和心臟移植)手術,器官移植包括血糖和胰島素水平明顯升高,骨髓移植或臍帶血幹細胞移植治療可部分改善患者癥狀,身體發育到得改善,但手術不能預防肝腺瘤的發生,器官移植並發癥多,死亡風險高.
五、對癥治療:對有心力衰竭、腎功能損害、營養缺乏和中性粒細胞減少而反復發生感染者均應采取相應的對癥治療.
六、藥物治療:維生素類藥物,如B族維生素維生素C等.有感染給抗生素治療.糾正低血糖後如果血脂仍繼續升高,可用安妥明50mg/(kg·d).高尿酸血癥如采用飲食療法不能控制時,可用別嘌呤醇5~10mg/(kg·d).激素治療有益於維持正常血糖水平、提高食欲.
預後
新生兒和嬰兒由於身體免疫系統發育不成熟,疾病較嚴重,治療難度大.年齡較大的兒童,具有一定的抵抗力,治療也較容易.本病為遺傳性疾病,故難以根治,但近些年發展起來的基因治療,有可能使糖原累積病得到根治.
糖原累積病 GDS 糖原累積病饮食
多以清淡食物為主,註意飲食規律.
糖原累積病 GDS 糖原累積病并发症
可並發乳酸血癥,酸中毒,酮尿,高脂血癥,感染,嚴重的可死於酸中毒或感染等疾病.
1/2 1 2 下一页 尾页