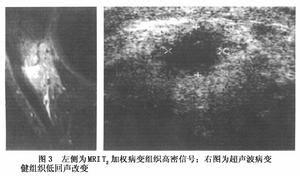
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥百科
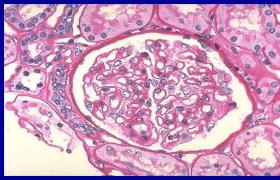
范科尼綜合征(Fanconisyndrome),別名:小兒綜合征,小兒戴佈二氏血虛,小兒凡科尼綜合征,小兒范科尼綜合癥,小兒范可尼血虛,小兒范可尼綜合征,小兒復合腎小管轉運缺陷癥.是由於近端腎小管對多種物質再吸收障礙,氨基酸、葡萄糖、磷酸鹽、碳酸氫鹽及其他物質自尿中大量丟失,導致近端腎小管酸中毒、低鉀血癥、佝僂病、骨質稀疏和生長發育遲滯等表現的一個綜合征.Fanconi綜合征(Fanconisyndrome)可分為先天性或獲得性,原發性或繼發性,完全性或不完全性幾類.臨床上較為罕見,起病緩慢,且多於青壯年出現癥狀,預後與治療早晚和對治療的反應有關.
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥病因
(一)發病原因
幼兒大多與遺傳有關,年長兒多繼發於免疫性疾病,毒物或藥物中毒以及各種腎臟病.
1.原發性(原因不明或無全身性疾病)包括遺傳性常染色體顯性(AD),常染色體隱性(AR),X連鎖隱性(XLR),散發性,特殊型(即刷狀緣缺失型).
2.繼發性(癥狀型)(1)先天性代謝障礙:①氨基酸代謝障礙:A.胱氨酸病(常染色體隱性,AR),B.酪氨酸血癥Ⅰ型(AR),C.Busby綜合征(AR),D.Ludersheldon綜合征(AD),②碳水化合物代謝障礙:A.糖原貯積病Ⅰ型(Fanconi-Bickel綜合征,AR),B.半乳糖血癥(AR),C.遺傳性果糖不耐受癥(AR),③其他:A.Lowe綜合征(XLR),B.肝豆狀核變性(AR),C.細胞色素C氧化酶缺陷(AR),D.Dent病(傢族性近端腎小管疾病,XLR),E.Pearson綜合征,Wilson病,F.維生素B12缺乏.
(2)獲得性疾病如:①多發性骨髓瘤;②腎病綜合征;③腎移植;④腫瘤;⑤糖尿病;⑥急,慢性間質性腎炎;⑦急性腎小管壞死;⑧營養不良;⑨巴爾幹腎病;⑩嚴重低鉀血癥.
(3)藥物損傷及中毒如:①重金屬(汞,鈉,鉛,鎘);②化學毒劑馬來酸,來蘇兒,甲苯,甲酚,硝苯等;③過期四環素,丙酸;④順鉑,IFostamide,氨基糖苷類抗生素,維生素中毒;⑤雷米替丁,西米替丁,中草藥如馬兜鈴腎損害等.
(二)發病機制
1.發病機制本病發病機制尚未完全清楚,有以下幾種可能:
(1)內流缺陷:管腔內向組織內流減少,見於刷狀緣缺失型.
(2)細胞內回漏到腎小管腔增加:如馬來酸中毒型.
(3)回流減少:通過基底側細胞膜回流減少,致細胞內物質堆積;影響回吸收,如Fanconi-Bickel綜合征.
(4)灌註增加:從血液向細胞灌註增加,通過細胞緊密連結處反流管腔增加,如細胞色素C氧化酶缺乏型,腎小管膜的輸送異常在病理組織學檢查中未見特異性表現,有實驗提示本征的細胞內ATP活性的轉運功能不全是由於磷酸鹽耗竭,引起細胞內腺嘌呤核苷酸降解,因而發生ATP消耗,本癥的病理生理學改變見圖1.
2.病理與病理生理隨著分子生物學的研究進展,已認識到FA的發生是一個復雜的病理生理過程,DNA損傷識別或修復缺陷是FA發生的關鍵,由於DNA的異常啟動瞭相關的病理機制.
(1)DNA交聯修復缺陷:FA細胞對能產生鏈內和鏈間交聯的雙功能交聯劑(如DEB,MMC,氮芥,環磷酰胺,順鉑等)敏感,DEB和MMC誘導的鏈內交聯修復使DNA鏈切開,雙鏈DNA同時損傷則沒有可用的模板進行修復,需通過非同源末端連接(NHEJ)修復,在FA細胞,非同源重組修復的保真性下降,導致細胞缺陷,相反,通過姊妹染色單體互換的同源重組在FA沒有缺陷,除瞭NHEJ異常,DNA損傷的識別也是受損的,使FA細胞在復制完成以後阻滯在G2期檢查點.
(2)FA細胞對氧的超敏性:一種理論認為,FA細胞是被蓄積的氧自由基損傷的,這些氧自由基是由以下誘變劑產生的,如:高氧張力,γ-射線,誘裂劑和產生活性氫氧根的藥物,FA細胞紅細胞過氧化物歧化酶(SOD)的水平降低,而白細胞SOD的濃度正常,也有紅細胞SOD,過氧化氫酶和谷胱甘肽過氧化酶水平正常而谷胱甘肽轉移酶水平上升的報道,在FA,成纖維細胞SOD的水平正常,Mn-SOD,過氧化氫酶和谷胱甘肽過氧化酶的濃度增加,因此有人提出氧化劑的作用可能限於造血系統,SOD或過氧化氫酶加入到FA的淋巴細胞培養中能減少斷裂的數量,其他的研究者發現SOD,過氧化氫酶或半胱氨酸可減少MMC誘導的斷裂,在高氧張力的情況下培養淋巴細胞導致一些FA細胞的任意斷裂的數量增加,正常細胞和加入MMC後的所有FA細胞均沒有增加,Clarke等研究瞭FA細胞的凋亡,顯示在5%氧濃度時暴露在MMC中與正常細胞相同,當20%氧濃度時則對MMC超敏,暗示對FA細胞的毒性作用是MMC產生的氧反應產物(ROS)引起的,而不是DNA交聯形成,FA的氧敏感性涉及控制ROS過度產生的復雜系統或耐受氧誘導損害的能力,除線粒體外,細胞內產生ROS很大程度上是由於細胞色素P450酶系統,有研究表明FANCC蛋白與NADPH細胞色素P450還原酶,FANCG蛋白與細胞色素P4502E1(CYP2E1)之間相互作用,這兩種酶都產生R0S,低氧張力和抗氧化劑被用於改善生長和減少FA細胞任意或MMC誘導的染色體斷裂.
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥症状
常見癥狀
無力反復感染代謝性酸中毒消瘦便秘低血磷多飲低血鉀多尿脫水
1.原發性Fanconi綜合征
是一種常染色體隱性遺傳疾病,診斷時的平均年齡男性是6.5歲,女性是8歲,發病年齡范圍從出生到48歲,男女比例1.2∶1,發病無種族或地區差異,一傢中可有兄弟姐妹多人發病,早期患者的診斷是在再生障礙性貧血(白血病或腫瘤)發生時做出的;最近認為,患者的同胞有陽性的染色體斷裂或有特征性軀體異常,就診者即使沒有貧血也可以做出FA的診斷,FA為一綜合征,臨床表現主要包括3方面:骨髓衰竭,各種發育異常和腫瘤易感性增加.
(1)Alter分型:根據血液學特點,Alter等於1991年把FA分為6個臨床亞型:①重型再生障礙性貧血,依賴輸血,雄激素無效或未接受雄激素治療,②重型再生障礙性貧血,依賴輸血,正接受雄激素治療,但療效不佳,③中,重度再生障礙性貧血,不依賴輸血,雄激素治療有效,④中,重度再生障礙性貧血,不依賴輸血,未接受雄激素治療或雄激素治療無效,⑤有骨髓衰竭的特征,如輕度貧血,粒細胞減少,血小板減少;大紅細胞,HbF增高,病情穩定,不需輸血和雄激素治療,⑥血象正常,HbF正常或輕度異常,不需輸血和雄激素治療.
(2)anconi綜合征不是全部具備上述3個特征,①嬰兒型:也稱急性型,特點有:A.起病早,6~12個月發病,B.常因煩渴,多飲,多尿,脫水,消瘦,嘔吐,便秘,無力而就診,C.生長遲緩,發育障礙,出現抗維生素D佝僂病及營養不良,骨質疏松甚至骨折等表現,D.腎性全氨基酸尿,但血漿氨基酸正常,E.低血鉀,低血磷,堿性酸酶活性增高,高氯血癥性代謝性酸中毒,尿中可滴定酸及NH4可減少,尿糖微量或增多,血糖正常,F.預後較差,可死於尿毒癥性酸中毒或繼發感染,②幼兒型:起病較晚(2歲以後),癥狀較嬰兒型輕,以抗維生素D佝僂病及生長遲緩為最突出表現,③成人型:特點有:A.10~20歲或更晚發病,B.多種腎小管功能障礙;如糖尿,全氨基酸尿,高磷酸鹽尿,低血鉀,高氯酸中毒,C.軟骨病往往是突出表現,D.晚期可出現腎功能衰竭.
(3)血液學異常:FA最重要的臨床特征是血液學異常,FA是遺傳性骨髓衰竭綜合征最常見的類型,AA,MDS和AML在純合子的發生率都顯著增加,患者出生時的血細胞計數是正常的,最早被檢測到的異常是大紅細胞癥,隨後出現血小板減少和中性粒細胞減少,40歲以前出現血液學異常的概率是98%,最常見的血液學異常是血小板減少和全血細胞減少,與骨髓增生低下有關,53%的患者以全血細胞減少發病,38%的患者以血小板減少發病,隨訪20年後有84%的患者發展為全血細胞減少,少部分患者以貧血,中性粒細胞減少發病,部分患者發病時即為骨髓增生異常綜合征(MDS)或急性白血病(尤其是急性髓系白血病),臨床上,FA患者有出血,蒼白和(或)反復感染.
(4)其他表現:身材矮小的FA患者28例檢測瞭生長激素(GH)水平,有22例GH缺乏,GH激素治療15例患者有12例長高,無一例患者造血改善,GH治療的患者中一例死於急性髓系白血病,最近報道44%的患者有GH缺乏,36%的患者有甲狀腺功能減低,重組GH在生長和造血中的作用還需要進一步觀察,而且GH治療和白血病之間的可能聯系需要仔細探討.
2.繼發性Fanconi綜合征
因病因不同,表現有所不同.
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥检查
1.血象
血常規檢查顯示三系呈不同程度下降,貧血屬正細胞正色素性,大紅細胞伴有輕度的異形性和紅細胞大小不均,網織紅細胞減少,但有時可高達3%,白細胞和中性粒細胞比例下降,血小板下降最早,一些患者紅細胞壽命縮短,胎兒血紅蛋白(HbF)水平增高達3%~15%.
2.骨髓象
骨髓象類似於獲得性再障,當發生再障時,FA患者的骨髓增生低下和脂肪化,造血成分減少,紅系和粒系比例下降,有時可出現紅細胞巨幼樣變,巨核細胞明顯減少,淋巴細胞,組織嗜堿細胞,網狀細胞等非造血細胞的數量相對增多.
3.激素水平
身材矮小的FA患者28例檢測瞭生長激素(GH)水平,有22例GH缺乏,GH激素治療15例患者有12例長高,無一例患者造血改善,GH治療的患者中一例死於急性髓系白血病,最近報道44%的患者有GH缺乏,36%的患者有甲狀腺功能減低,重組GH在生長和造血中的作用還需要進一步觀察,而且GH治療和白血病之間的可能聯系需要仔細探討.
4.診斷性實驗室檢查
診斷性檢查是染色體斷裂,用植物血凝素刺激培養的外周血的淋巴細胞,FA患者的細胞斷裂,裂隙,重排,互換和核內復制的比例高,當加入誘裂劑如DEB或MMC時,這些染色體異常則顯著地增加,FA純合子的外周血淋巴細胞加DEB培養後每個細胞平均有8.96個斷裂,正常細胞平均有0.06個斷裂,另外診斷FA的方法是流式細胞儀,FA患者細胞生長緩慢是由於細胞周期的G2期延長,用烷化劑治療的細胞不能分裂,但有染色體復制和在G2期的蓄積,由於含有DNA的量增加因此能被檢測.
5.其他
半數病人出現氨基酸尿,以脯氨酸尿為多見,紅細胞生成素的水平在FA患者增加,紅細胞長期存在i抗原(正常人2歲前消失),X線檢查,包括胸片和骨片檢查;B超或超聲心動圖檢查等各種影像學檢查,根據臨床需要選擇,X線檢查可發現骨質疏松,佝僂病表現;胱氨酸儲積病者,眼裂隙燈檢查可見角膜有胱氨酸結晶沉著等.
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥预防
本癥病因不明,可能系胚胎期受病毒感染和理化因素等外界致病因素影響而造成遺傳基因變異和染色體異常,導致骨髓造血幹細胞損傷和其他先天畸形,同此,應重視孕期保健,積極防治各種感染,尤其是病毒感染性疾病,避免理化因素,毒性物質的損害.
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥治疗
(一)治療
1.病因治療
對代謝缺陷類型已被認識的繼發性Fanconi綜合征,可進行特異性治療,通過飲食療法減少或避免有毒代謝產物積聚的疾病有半乳糖血癥,遺傳性果糖不耐受,酪氨酸血癥Ⅰ型,通過促進排泄治療的疾病有Wilson病和重金屬中毒,由藥物引起的Fanconi綜合征,清除體內藥物可糾正腎小管功能障礙,堅持,恰當地進行特異性治療,可使患者完全恢復正常,對於由腎臟疾病或全身疾病後引起的Fanconi綜合征則相應針對原發病治療.
2.對癥治療
(1)糾正酸中毒根據腎小管受損的程度給予堿性藥物,劑量2~10mmol/(kg·d),可采用碳酸氫鈉或者枸櫞酸鈉鉀合劑,全天劑量分4~5次口服,然後根據血中HCO3-濃度調整劑量,應註意同時補鉀,如堿性藥物用量過大,可合用氫氯噻嗪,促進HCO3-回吸收.
(2)糾正低磷血癥:口服中性磷酸鹽以糾正低磷血癥,劑量為1~3g/d,分次服,每4~5小時用藥1次,不良反應有胃腸不適和腹瀉,減少用量可減輕上述癥狀,在部分患者,應用磷酸鹽可加重低鈣血癥,誘發甲狀旁腺功能亢進,可口服鈣劑和維生素D預防,中性磷酸鹽配方:Na2HPO4·7H2O145g,Na2HPO4·H2O18.2g,加水至1000ml,每1000ml供磷2g.
(3)其他:應補充血容量,防脫水,糾正低鉀血癥,對於低尿酸血癥,氨基酸尿,糖尿及蛋白尿,目前尚缺乏有效的治療方法,腎功能不全者,則酌情采用保守式腎臟替代治療,FA的治療主要針對其血液學改變以及危及生命的各種並發癥.
3.雄激素和皮質類固醇激素治療
當FA患者發生全血細胞減少時,治療主要是雄激素和支持治療,雄激素可增加EPO的產生,刺激紅系幹細胞,從而提高血紅蛋白水平,約75%的患者雄激素治療有效,雄激素起效最早的表現是出現大紅細胞以及HbF水平增加,開始治療後2~3個月血紅蛋白開始上升,隨後血小板計數上升,最後中性粒細胞上升,要確定雄激素是否有效至少要堅持用藥6個月以上,有效時間可持續幾個月至20年不等,幾乎所有的患者停用雄激素後復發,僅少數治療時小於12歲的患者,在青春期時可停止治療而不復發,最終許多患者對所用的雄激素耐藥,換用另外一種雄激素少部分患者可能有效,由於雄激素的應用,延長瞭患者的生存期,但一些患者可能出現腫瘤等晚期並發癥,單獨應用雄激素與雄激素加皮質類固醇激素的療效相同,但一般推薦聯合治療,皮質類固醇激素引起的生長遲緩可抵消雄激素使生長加速的副作用,也可以通過降低血管的通透性減少出血,最常用的雄激素是司坦唑(康力龍),口服0.1mg/(kg·d),潑尼松(強的松)5~10mg,隔天1次,為降低肝臟毒性可用雄激素註射劑,苯丙酸諾龍(長效多樂寶靈)1~2mg/(kg·周),肌內註射,為預防血腫,可用冰袋冷敷和按壓,雄激素的副作用有女性男性化,多毛癥以及聲音變粗,外生殖器肥大,痤瘡,情緒不穩,水,鈉瀦留,體重增加,肌肉發達,由於骨骼成熟加速致骨骺過早融合,最終導致身材矮小,這些副作用中部分在雄激素減量或停用後消失,比較嚴重的副作用包括肝大,膽汁鬱積性黃疸和肝功能中轉氨酶水平上升,但這些是可逆的,最嚴重的問題是肝紫癜,肝腺瘤和肝細胞癌,但這些在雄激素治療停止後也能恢復,接受雄激素治療的患者需定期進行肝生化檢查和超聲檢查,治療有效的患者可逐漸減量但不能停藥,但有些患者雄激素可停用,這些患者可能有血液系統鑲嵌現象,其“正常”幹細胞有選擇性造血優勢.
4.細胞因子
造血生長因子如非格司亭(G-CSF)和莫拉司亭(GM-CSF),能改善造血,特別是中性粒細胞減少的患者,能增加中性粒細胞絕對值,僅少數患者血紅蛋白和血小板計數增加,可與雄激素聯合應用或用於雄激素治療無效的患者,然而,這些因子的應用也能使腫瘤易感的患者發生白血病或促使向MDS或7號染色體單體演化,因此僅用於嚴重中性粒細胞減少的患者,慎用於有克隆性細胞遺傳學異常的患者,並註意監測外周血細胞計數,定期行骨髓檢查和骨髓細胞遺傳學檢查,一旦發現異常應停用.
5.造血幹細胞移植
造血幹細胞移植是惟一能治愈FA患者的措施,也可以預防白血病的發生,HLA相合的同胞供者異基因骨髓移植,兩年生存率可達到66%;無HLA相合的同胞供者可選擇HLA相合的無關供者或不匹配的傢族成員,但移植效果很差,兩年生存率僅29%,HLA相合的同胞臍帶血移植已有成功的報道,但需行著床胚胎遺傳學診斷,以確定胚胎無FA傾向且與患者HLA相合,為獲得HLA相合的同胞臍帶血,需多次嘗試,造成瞭大量的無FA傾向但HLA不相合的胚胎的浪費,這在倫理學上是有爭議的,無關臍帶血移植效果差,由於FA患者對放療和預處理方案藥物如環磷酰胺(CTX)超敏,可發生嚴重的黏膜炎伴有腸道吸收障礙和出血,液體瀦留,心功能衰竭及出血性膀胱炎,減少環磷酰胺(CTX)的劑量到20mg/kg,分4天給藥,加5Gy的胸腹部放療,這個方案的累積生存率大約是70%,應用氟達拉濱進行預處理,代替放療取得瞭更好的療效,盡管骨髓移植是一種有效的治療措施,但化療和放療增加瞭發生第二腫瘤的危險(尤其是頭頸部腫瘤).
6.基因治療
FA前體細胞和肝細胞的基因轉導可以從遺傳學上糾正所有系統的造血細胞異常,恢復正常的持續造血,在FAA和FAC患者的體外試驗中均已獲得成功,是目前FA基因治療的依據所在,應用反轉錄病毒介導的基因轉移,矯正FANCC敲除的小鼠對MMC的高敏性,已有成功的報道,在人類應用反轉錄病毒載體的臨床試驗還未成功,但最近用慢病毒載體在敲除瞭基因的小鼠取得瞭較好的結果,應用少量的病毒就能獲得有效的轉導,不需要預先應用細胞因子而且體外操作極少,因此用於人類的治療可能比反轉錄病毒更成功.
7.其他治療
合並再生障礙性貧血的FA患者均需要支持治療,有出血的患者,可用氨基己酸0.1g/kg,每6小時服用1次,有可能進行移植治療的患者,應避免輸註來自傢族成員的血液制品,以減少移植時過敏的可能,過濾瞭白細胞的血液制品可減少輸血反應和對白細胞過敏,避免接觸可引起獲得性再生障礙性貧血的藥品和化學物質,血小板減少的患者避免應用影響血小板功能的藥物,脾切除術隻用於巨脾的患者,對長期預後沒有明顯的益處,大劑量的甲潑尼龍(甲基強的松龍),抗胸腺細胞球蛋白和環孢素曾用於FA患者的治療,但缺乏療效,FA繼發AML的治療困難,預後差,由於DNA修復缺陷,對化療敏感性增加,因此化療相關毒性增加,化療劑量應減少,抗氧化劑治療亦有報道,但在嘗試中.
(二)預後
本病預後取決於所累及的臟器以及治療開始的早晚,持續性和原發病等因素,嚴重患者最終多死於嚴重水,電解質紊亂及腎功能衰竭.
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥饮食
范科尼(Fanconi)綜合征是一種遺傳性或獲得性疾病.常與胱氨酸病相伴發,故需在飲食上多註意.飲食中的蛋氨酸在體內代謝後轉為胱氨酸,故胱氨酸結石患者應采用低蛋氨酸飲食,比如蛋、禽、魚、肉等.水果、蔬菜能使尿液轉為堿性,對防止胱氨酸結石較好,並多飲水以減少胱氨酸濃度而達到治療的作用.
小兒范科尼綜合征 小兒Fanconi綜合征 小兒戴-佈二氏貧血 小兒凡科尼綜合征 小兒范科尼綜合癥 小兒范可尼血虛 小兒復合腎小管轉運缺陷癥并发症
1.並發癥
常並發發育障礙,抗維生素D佝僂病及營養不良,骨質疏松甚至骨折,低血鉀,低血磷,高氯血癥,死於尿毒癥性酸中毒或繼發感染.
2.多伴發先天性畸形
在嬰兒期診斷的FA患者有較高的比例有特征性軀體異常,如畸形包括拇指和橈骨,腎臟,頭,眼睛和耳朵以及胃腸道畸形,相反,在年長兒診斷的FA患者,軀體異常少見,身材矮小和皮膚色素問題隨著年齡增加而顯現出來,FA患者的典型異常包括:身材矮小,拇指或橈骨不發育或缺如或多指,小眼球,小頭畸形,皮膚色素沉著,淺褐色斑和色素脫失斑,以及特征性面部表現如鼻基底部增寬,眥上皺襞和小頜,大約1/3的患者有腎臟異常,包括腎發育不全,馬蹄形腎或雙輸尿管,生殖系統發育不全(女性月經來潮較晚,月經不規則,絕經早,婦科腫瘤多;男性性腺,尿道發育不完全),少見的異常包括胃腸道,心臟和中樞神經系統等部位的缺陷,隻有血象和骨髓象異常的而無先天畸形的患者稱為Estren-Dameshek綜合征,這些患者僅代表FA范疇中的一部分.
3.腫瘤易感性
FA患者發生白血病和腫瘤的報道多於200例,總的發生率大於15%,急性白血病占100例以上,占FA患者的10%,主要是急性髓系白血病,發生MDS的危險是10%~35%,有克隆性細胞遺傳學異常的患者發生MDS或AML的危險明顯高於染色體核型正常者,克隆性細胞遺傳學異常累及染色體1和7,其他的異常包括染色體部分或完全的缺失,易位和標記染色體,FA患者發生實體瘤的危險性隨年齡的增大而增加,大多數是鱗狀細胞癌,最常累及消化道和女性生殖系統.
4.FA異質性
在FA患者的親戚中可發現先天性畸形,泌尿生殖系統和手的特殊異常,一些FA患者的父母親有身體畸形如身材矮小,但沒有血液學疾病,Pefidou和Barrett註意到有關的異質性有HbF水平的增加,自然殺傷細胞數量的減少和對絲裂黴素反應差,FA的異質性也可以通過染色體斷裂分析被檢測.
1/2 1 2 下一页 尾页